- 先週、アステラス製薬株式会社とファイザー株式会社は、筋浸潤性膀胱癌に対する PADCEV+KEYTRUDA、HER2+ 転移性乳癌のファーストライン治療に対する TUKYSA を含む、極めて重要な第 3 相試験の良好な結果を発表しました。
- これらの重要な試験結果は、ファイザーのがん領域のポートフォリオにおける重要な進歩を反映したものであり、現在利用できる治療法が限られている患者に対するがん治療の選択肢を改善する可能性を強化するものです。
- 膀胱がんと乳がんにおける強力な第3相試験の結果が、ファイザーの投資見通しと将来の業績予想にどのような影響を与える可能性があるかを検証する。
最新のGPUは、ジスプロシウムと呼ばれる希土類金属の一種を必要とし、それを探索または生産している企業は世界で36社しかない。無料でリストを検索
ファイザー投資シナリオのまとめ
ファイザーの長期的な魅力は、そのイノベーション・エンジンとグローバル・リーチへの信頼にあり、後期がん治療薬やその他の画期的新薬の進歩が、迫り来る特許切れや価格設定の逆風という高まる圧力に打ち勝つことができるという期待がある。最近のPADCEV、KEYTRUDA、TUKYSAの良好な第3相試験結果は、パイプラインの実行を確認するものであるが、規制および競合リスクの変化の遅さを考慮すると、このニュースは、新薬承認のペースという短期的な主要触媒や、米国および世界的な薬価制度改革という最大のリスクを大きく変えるものではない。
最近の発表の中で、ファイザーが348回連続の四半期配当を宣言したことは、株主にとって際立っている。最新のがん領域のデータとは無関係ではあるが、好調で安定した配当は、経営上の移行期や規制上の不確実性のある時期において、時として支えになることがある。
しかし、パイプラインの勢いとは裏腹に、多くの投資家が見逃しているのは、...
ファイザーのシナリオでは、2028年までに売上高596億ドル、利益128億ドルを見込んでいる。これは、現在の収益107億ドルから年間2.2%の減収と21億ドルの増益を必要とします。
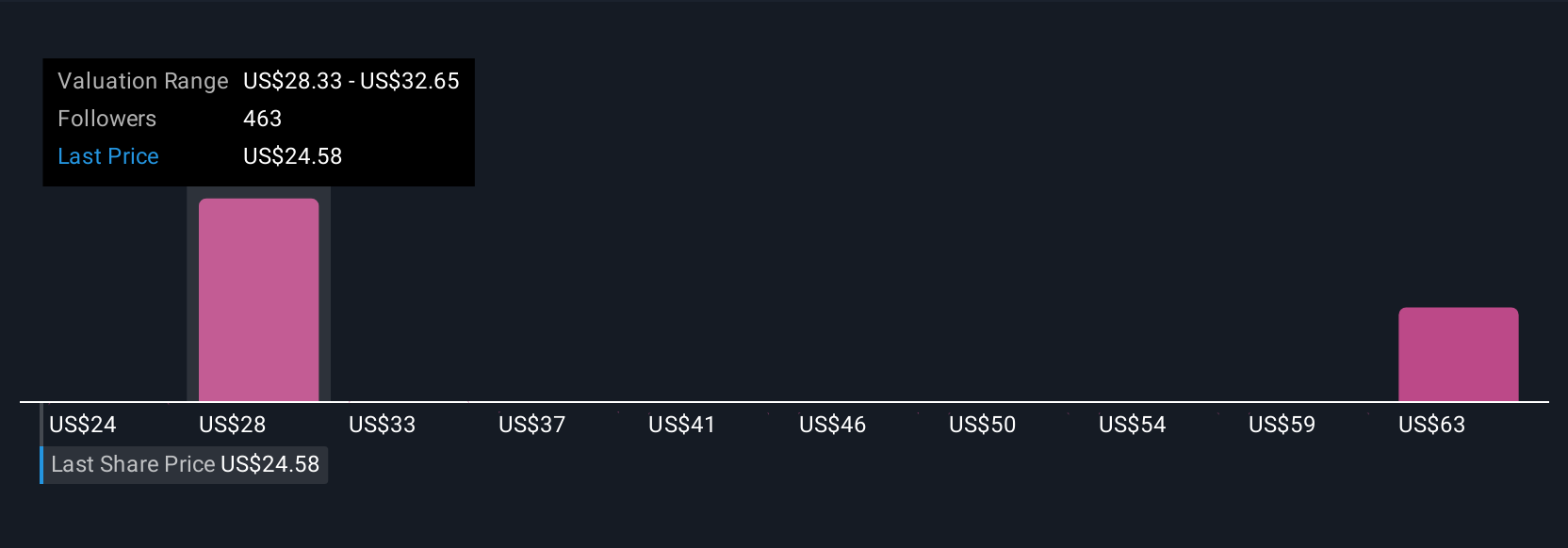
ファイザーの予測から、フェアバリューは28.86ドルとなり、現在の株価から18%のアップサイドとなります。
他の視点を探る
大半のアナリストは、ファイザーの売上高が2028年までに655億米ドル程度に若干落ち込むと予想しているが、最も楽観的なアナリストは、今週のがん領域のニュースのように、迅速な新治療の承認が成長を加速させる可能性があると信じている。より迅速な薬事規制や世界的な普及を信じるなら、あなたの見通しはコンセンサスよりもはるかに強気かもしれません。
ファイザーの他の37のフェアバリュー予想- なぜ株価は現在価格の2倍以上の価値があるのか - をご覧ください!
独自のファイザー物語を構築する
既存のシナリオにご不満ですか?3分以内に独自のシナリオを作成 - 群れに従うことで並外れた投資リターンが得られることはめったにありません。
- ファイザー調査の出発点として、投資判断に影響を与える可能性のある4つの重要な報酬と2つの重要な警告サインを強調した当社の分析が最適です。
- 当社の無料 Pfizer リサーチ レポートは、包括的なファンダメンタル分析を単一のビジュアル (スノーフレーク) にまとめたもので、Pfizer の全体的な財務の健全性を一目で簡単に評価することができます。
他の投資をお探しですか?
毎日が大切です。これらの無料ピックはすでに注目を集めています。群衆より先にご覧ください:
- リスクとリターンのバランスが取れた、財務的に健全なペニー株で、次の大物を発掘しましょう。
- がんの終焉?がんやアルツハイマーなど、人生を変える病気の早期発見を可能にする技術を開発している28の新興AI銘柄を紹介。
- 次世代技術の革命をリードし、量子アルゴリズム、超伝導量子ビット、最先端研究のブレークスルーで未来を形作る量子コンピューティングのトップ企業26社を探る。
本記事は一般的な内容です。当社は、過去のデータとアナリストの予測に基づき、偏りのない方法論のみで解説を行っており、当社の記事は財務アドバイスを意図したものではありません。また、お客様の目的や財務状況を考慮するものではありません。弊社は、ファンダメンタルズ・データに基づく長期的な焦点に絞った分析をお届けすることを目的としています。 弊社の分析は、価格に影響を与える最新の企業発表や定性的な材料を織り込んでいない可能性があることにご留意ください。 Simply Wall Stは、言及されたいかなる銘柄にもポジションを有していません。
評価は複雑だが、我々はそれを単純化するためにここにいる。
公正価値の見積もり、潜在的リスク、配当、インサイダー取引、財務状況など、詳細な分析により、Pfizer が割安か割高かをご確認ください。
無料分析へのアクセスこの記事についてご意見をお持ちですか?内容に懸念がありますか?当社まで直接ご連絡ください。 または、editorial-team@simplywallst.comまでメールをお送りください。
This article has been translated from its original English version, which you can find here.
